半世紀来の謎だったセファロスポリン系抗菌薬が薬によって多様な血漿タンパク結合率を示す理由を原子レベルで解明
藤田医科大学 医学部 河合 聡人 講師、土井 洋平 教授、崇城大学 薬学部 山﨑 啓之 教授、小田切 優樹 特任教授の共同研究グループは、実臨床でも使用頻度が高いセファロスポリン系抗菌薬セフトリアキソン及びセファゾリンとヒト血清アルブミン(HSA)との相互作用解析を実施し、似た構造を有するセファロスポリン系抗菌薬が薬によって異なる血漿タンパク結合率を示す要因を原子レベルで解明しました。
本研究成果は、8月1日(日本時間)に米国化学会が出版している学術ジャーナル「Journal of Medicinal Chemistry」のオンライン版に掲載されました。
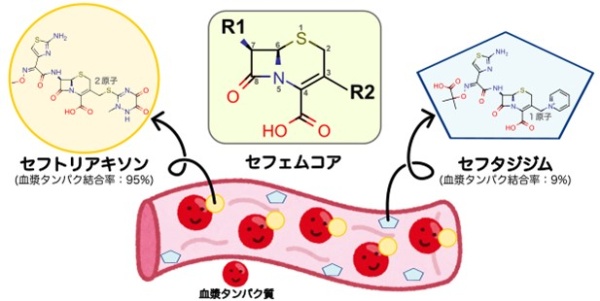
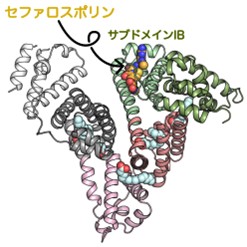
図2 セフトリアキソンとHSA複合体の立体構造
a
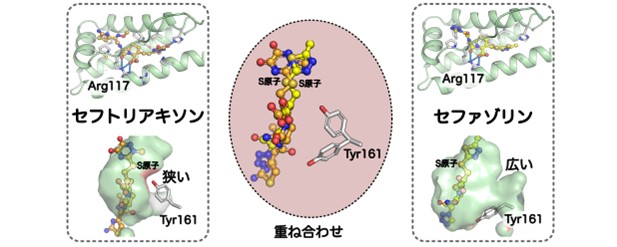
図3 セフトリアキソン及びセファゾリンの結合部位
下:結合ポケット内の空間を着色しました。
本研究はJSPS科研費JP20K16060の助成を受けて実施しました。また、放射光X線回折実験は高エネルギー加速器研究機構放射光科学研究施設共同利用実験(2017G554、2019G592)として、Photon Factory BL-1AおよびBL-17Aにて行いました。
2. 藤田医科大学 感染症研究センター
3. 崇城大学 薬学部
4. 崇城大学 DDS研究所
5. Division of Infectious Diseases, University of Pittsburgh School of Medicine
本研究成果は、8月1日(日本時間)に米国化学会が出版している学術ジャーナル「Journal of Medicinal Chemistry」のオンライン版に掲載されました。
研究成果のポイント
- 実臨床での使用頻度が高く、血漿タンパク結合率が高いセファロスポリン系抗菌薬セフトリアキソン及びセファゾリンとHSAの相互作用解析を実施。
- X線結晶構造解析、HSA結合競合実験、薬剤感受性試験により、セファロスポリン系抗菌薬の結合部位はHSAのサブドメインIBに存在し、セファロスポリンのR2側鎖を収納する結合ポケットの形状への適合度によって各種セファロスポリン系抗菌薬の血漿タンパク結合率が異なることを解明。
背景
セファロスポリン系抗菌薬はペニシリンと同じβ-ラクタム系抗菌薬の仲間で、セファロスポリンCが開発された1960年代から今日までに数多くの薬が開発され、現在でも20種類以上が細菌感染症の治療に用いられている代表的な抗菌薬です。セファロスポリン系抗菌薬は、 “セフェムコア”と呼ばれる共通構造を有し、その構造の3位と7位に結合する側鎖構造(3位:R2側鎖、7位:R1側鎖)を変えることで、効果のある細菌種のスペクトラムを拡大させ、且つ、抗菌薬へ耐性を示す細菌にもより効果が得られるように開発されてきました(図1 中央)。その結果、セファロスポリン系抗菌薬は同じような化学構造の薬でありながら、グラム陽性菌に強い薬、グラム陰性菌に強い薬といった特徴があり、感染症の起因菌や感染部位に合わせて使い分けられています。さらに、セファロスポリン系抗菌薬は薬によって血液中での血漿タンパク質への結合割合が異なり、加えて血漿タンパク結合率の高いセファロスポリン系抗菌薬はHSAに結合していることが知られていました。一般的に薬は血液を介して全身を巡りますが、血漿タンパク結合率が高い薬は血液中で血漿タンパク質と結合した状態で存在するため、比較的長時間体内に留まることができます。一方で薬は血漿タンパク質と結合していない状態で薬効を発揮すると考えられています。このことから、安全に薬を使用するためにはこの血漿タンパク結合を考慮して薬の投与量、頻度を決める必要があり、血漿タンパク結合率は薬の取り扱い説明書である添付文書にも記載される項目です。実際、セファロスポリン系抗菌薬の中でも血漿タンパク結合率が高いセフトリアキソン(血漿タンパク結合率:95%、図1左)は体内の貯留時間が長く、1日1回の投与で治療効果が見込める薬ですが、肝疾患や腎疾患などで低アルブミン血症を呈した患者ではHSAが減少したことで血液内に留まれず、体内からの消失が早くなり、血中アルブミン濃度が平常な人と同様に投与すると治療効果の期待できる血中濃度を維持できないことが報告されています。一方で、セフトリアキソンと同時期に開発されたセフタジジムは血漿タンパク結合率が低く(血漿タンパク結合率:9%、図1右)、治療効果に血中アルブミン濃度の影響は少ないようで、薬の排泄を担う腎機能を基準に投与設計することが推奨されています。このように、セファロスポリン系抗菌薬は薬によって血漿タンパク結合率が異なり、薬の使用において注意すべき項目が変わることは知られていましたが、「似た構造の薬なのになぜ血漿タンパク結合率が異なるのか?」という化学的な謎については未解明のままでした。
図1 セファロスポリン系抗菌薬の構造と血液内でのイメージ
研究手法・研究成果
研究グループはまず血漿タンパク結合率の高いセファロスポリンがHSAのどの場所に結合するのかを調べるために、HSAとセフトリアキソン及びセファゾリン(血漿タンパク結合率:80%)の共結晶を調製し、茨城県つくば市にある高エネルギー加速器研究機構の放射光実験施設Photon Factory BL-17Aビームラインを利用してX線結晶構造解析法による立体構造の決定を行いました(図2)。その結果、セフトリアキソン及びセファゾリンは共にHSAのサブドメインIBに存在するトンネル状の窪み1ヶ所に結合していることがわかりました(図2及び図3)。次にX線結晶構造解析で観察された結合部位が溶液中でも同じであることを確認するため、薬剤感受性試験とHSA結合競合実験を実施しました。HSAを添加した培地でセフトリアキソンの薬剤感受性試験を実施すると最小発育阻止濃度(MIC)が上昇することが知られていましたが、HSAサブドメインIBに結合することが知られている薬(ビカルタミド)を培地に追加するとその量依存的にMICの上昇が軽減されました。また、セフトリアキソンのHSAに対する結合定数もビカルタミドの量依存的に低下したことから、溶液中でもセフトリアキソンはHSAのサブドメインIBに結合していることが確認できました。そこで立体構造に戻り、セフトリアキソン及びセファゾリンとHSAの相互作用の詳細を観察すると、共通して窪みの中心にあるArg117残基の側鎖とセフェムコアの4位のカルボキシル基及び8位のカルボニル基が水素結合を形成し、セファロスポリンのR1及びR2側鎖はトンネルを貫通するように窪みに収まっている様子が観察されました(図3上)。さらにこれらの構造を重ねて比較すると、セフトリアキソンが結合したHSAの構造ではTyr161残基の配向が異なり、R2側鎖を収納している部位が局所的に狭くなっていることがわかりました(図3下)。また、この構造変化はセフトリアキソンのR1側鎖が分岐した嵩高い構造をしていることが原因で、両者の立体障害を解消するために起ったものと推測されました。これに注目して、他のセファロスポリン系抗菌薬の化学構造を観察してみると、R1側鎖の構造はセフトリアキソンと同様に分岐した嵩高い構造を有している薬が多いことがわかりました。また、セフェムコアからR2側鎖が結合している部分に注目すると、血漿タンパク結合率が高い薬はセフェムコアとR2側鎖を繋ぐリンカーが2原子で構成されているのに対し、血漿タンパク結合率が低い薬はリンカーが1原子と短いことがわかりました(図1)。加えて、R2側鎖が無い、またはメチル基や塩素原子のような小さなものは中間の血漿タンパク結合率を示していたことから、血漿タンパク結合率が高いセファロスポリン系抗菌薬はTyr161の回転による狭窄部分を回避してR2側鎖が収まるポケットと相互作用できる構造を有している薬で、続いてR2側鎖が小さい薬、R2側鎖が狭窄部分とぶつかる構造を有する薬の順に血漿タンパク結合率が低下していることがわかりました。
図2 セフトリアキソンとHSA複合体の立体構造

図3 セフトリアキソン及びセファゾリンの結合部位
下:結合ポケット内の空間を着色しました。
今後の展開
本研究で血漿タンパク結合率の高いセファロスポリン系抗菌薬のHSA中の正確な結合位置、その相互作用が明らかになり、各セファロスポリン系抗菌薬の血漿タンパク結合能の違いに関する化学的理由が解明されました。治療中のセファロスポリン系抗菌薬の血中濃度は血液中のHSA濃度と同等にまで到達するものも多く、HSAに結合する他の薬へ影響することが危惧されます。加えて感染症はいつ罹患するかわからず、また迅速な治療が求められることから、本研究成果を基礎データとして、今後、日頃から服用している薬と一緒に使用される場面を想定して、HSAの結合部位で競合する薬の組み合わせとその影響を調べていくことでより安全な感染症治療に繋がるものと考え、研究を進めていきます。本研究はJSPS科研費JP20K16060の助成を受けて実施しました。また、放射光X線回折実験は高エネルギー加速器研究機構放射光科学研究施設共同利用実験(2017G554、2019G592)として、Photon Factory BL-1AおよびBL-17Aにて行いました。
文献情報
論文タイトル
Interaction of Cephalosporins with Human Serum Albumin: A Structural Study著者
河合 聡人1,2, 山﨑 啓之3,4, 小田切 優樹3,4, 土井 洋平1,2,5所属
1. 藤田医科大学 医学部2. 藤田医科大学 感染症研究センター
3. 崇城大学 薬学部
4. 崇城大学 DDS研究所
5. Division of Infectious Diseases, University of Pittsburgh School of Medicine
